Заготовка трахеи напоминает экспонат для музея.
Капилляры, клетки головного мозга и нервной системы, клапаны сердца, фрагменты печени. Дальше — больше. Мочевой пузырь, мочевые протоки, роговица глаза, новое сердце на каркасе старого – биомедики во всем мире экспериментируют на животных и людях, выращивая не только ткани, но и органы. Основа революционного направления – стволовые клетки и 3D-печать. А как же регенеративная медицина развивается в нашей стране?
Кожная «заплатка»
Скоро впервые пациентам пересадят образцы «искусственной» кожи. Их выращивают специалисты РНМЦ «Клеточные технологии». Ожидается, что с помощью новой разработки раны и ожоги будут заживать быстрее и более эффективно. Как же кожа человека созревает вне человека? Заглянем в лабораторию.
Читайте также
Технолог работает в ламинарном боксе, ограниченном стерильном пространстве. Кладет под увеличитель микроскопа пластиковый флакончик с рубиновой жидкостью. Это питательная среда, где размножаются невидимые глазу клетки кожи. Она содержит все, что нужно для роста: аминокислоты, белки, гормоны. За два месяца базовый кусочек кожи прирастает миллионами клеток! И выживают из них самые полноценные.
— Клеточная масса постепенно накапливается, — для ведущего научного сотрудника лаборатории молекулярной биологии клетки Зинаиды Квачевой этот мир вполне осязаемый. — Полученная из клеток суспензия наносится на раневые покрытия с коллагеном.
Что же получит в лаборатории врач? Выращенная кожа — это не «латка» на место ожога телесного цвета. У доктора на руках окажется биодеградируемое покрытие для раны, пропитанное слоями готового биомедицинского клеточного продукта.
— Доктор покроет этим материалом рану, — Зинаида Болеславовна предполагает, как будет происходить применение технологии на практике. — Клетки встроятся и начнут мигрировать, инициировать рост трансплантированных и собственных клеток в организме пациента. А покрытие-сеточка с коллаген-хитозановым комплексом потом распадется. И в течение двух месяцев рана зарастет уже видимой глазу кожей. Это персонализированная медицина, когда тканевый эквивалент готовится для конкретного пациента из его же клеток, но только модифицированных молодых стволовых.
Однако выращивание кожи из биоматериала больного — дело долгое. Клетки растут больше месяца. Поэтому сейчас в Минздраве рассматривают разрешение на использование донорской основы. Клетки донора, прошедшие через культуру, не вызывают отторжения. Специалисты считают, что это перспективное направление.

Технолог контролирует жизнь клеток.
Мертвое стало живым
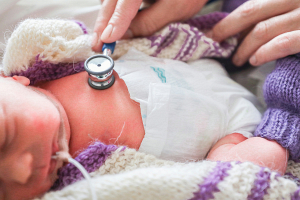
Анатолию Хлопкову из Рогачева врачи обещали максимум два месяца жизни. Рак легкого пророс в трахею и не оставлял шансов. Пациент уже плохо дышал. Остатки жизни в нем поддерживала терапия. Но после того момента, как Анатолию поставили диагноз, несовместимый с жизнью, он живет уже два года. Дни Анатолия Хлопкова продлила уникальная многоэтапная операция. Такой комплекс наши специалисты применили впервые в мире. Больному с онкологией пересадили трахею, выращенную специально для него. Каждые три месяца он проходит обследование в Республиканском центре онкологии и медицинской радиологии имени Н.Н. Александрова. По словам врачей, все у больного хорошо.
Пока нуждающихся в такой операции нет, но специалисты в любой момент готовы повторить биомедицинский подвиг. Мы отправились в Республиканскую молекулярно-генетическую лабораторию канцерогенеза, чтобы узнать, как же выращивают трахею для пересадки.
Заведующая отделением клеточных технологий Татьяна Дорошенко открывает холодильник. В стеклянных сосудах трахеальные трубки цвета слоновой кости. Перед нами образцы очищенного дыхательного горла, забранные от собаки и человека. Так по-другому называют важную часть дыхательных путей, которая соединяет гортань и бронхи. Для глаза они почти одинаковые. Чтобы точно узнать, кому принадлежит трахейный хрящ, надо заглянуть в журнал учета. Единственный признак для сведущего – у собаки трахеальная трубка чуть длиннее. Именно на ней, а также на дыхательном горле крыс и кроликов сотрудники лаборатории поставили первые эксперименты. По итогу масштабной работы с животными методику подготовки органа к пересадке усовершенствовали и применили на человеке.
Лучевая и химиотерапия против пожирающего трахею рака бессильна. Поэтому Анатолий Хлопков стал первым пациентом с искусственно выращенным дыхательным горлом. Как же оно росло?
Трахею забрали у трупного донора. Хрящевой слой трахеальной трубки выстилают клетки, провоцирующие реакцию отторжения у реципиента. И первая задача — смыть элементарные единицы строения трахеи умершего человека, остаточные частички чужой жизни.
— Дыхательное горло — самый грязный орган, — Татьяна Михайловна знает, о чем говорит. Это в банке заготовка выглядит как экспонат для музея анатомии. Сотрудники лаборатории приняли окровавленный кусок плоти, в котором еще теплилась чья-то жизнь. И микроорганизмы. Они оседают в трахее, проникая через дыхательные пути. Донорскую трубку предстояло отмыть от клеток хозяина и микробов. А потом оживить в организме реципиента.
— Мы взяли каркас, хрящ от неживого донора, — заведующая отделением клеточных технологий проходится по этапам этого сложнейшего вмешательства. — Пока никому не удалось воссоздать полностью композиционно трахею на основе искусственного материала, чтобы она по растяжению и устойчивости к сжатию не уступала природному органу.
Каркас промывали в очень жесткой концентрации антибиотиков. Донорскую трахею «купали» две недели в специальных компонентах. Над ней дрожала вся лаборатория.
Читайте также
Тем временем из спинного мозга пациента выделили мезенхимальные стволовые клетки.
— У них большой потенциал, — поясняет тонкости метода Татьяна Дорошенко. — Они способны дать хрящевую ткань, нервную, жировую. Все зависит от условий культивирования. Клеткам Анатолия Хлопкова задали развитие в сторону хрящевой ткани.
— Сегодня нет возможности обеспечить в пробирке прорастание сосудов в орган, — обращает внимание заведующая отделением клеточных технологий. — Поэтому профессор Владимир Жарков предложил пересадить хрящ с имплантированными клетками сначала в мышцу живота реципиента. В его теле трансплантат находился полтора месяца. Благодаря этому питание клеток улучшилось, а риск отторжения сошел на нет. Так трахеальная трубка ожила. А дальше была кульминация многоэтапного вмешательства. Анатолию удалили опухоль и пересадили новую трахею. Теперь она ему родная.

Кожа растет вне тела.
Сердце на принтереЗD-печать еще один путь искусственного создания органов. Заведующий лабораторией синтеза и анализа микро- и наноразмерных материалов Института тепло- и массообмена Сергей Филатов видит это так:
Читайте также
Пока же у нас печатают только шаблоны органов, для того чтобы отработать тончайшие нюансы будущей операции. Прототип, выполненный с помощью ЗD-моделирования и ЗD-печати, «заточен» под конкретного больного.
Если печать органов — отдаленная перспектива, то выращивать ткани планируют уже в этом году. Эту технологию будут претворять в жизнь специалисты Института тепло- и массообмена имени А.В. Лыкова и центра «Клеточные технологии».
— Наша первоочередная задача — создать мощный 3D-принтер, — говорит Сергей Филатов. — Такой, как в Сколково, который позволит начать работу. Мы отвечаем за техническую часть. А биологи займутся клеточным материалом. Им можно будет заселять напечатанную полимерную основу. Клетки могут загружаться во время печати и после.
Дефицит донорских органов будет всегда. К счастью, люди повально не падают замертво от инсульта и не гибнут в катастрофах. Но рядом те, кто страдает от неизлечимых болезней и ждет пересадки как единственного шанса на спасение. Ученые бьются над тем, чтобы создать эквиваленты жизненно важных частей тела для пересадки. Многое создано. У нас выращивают трахею, кожу, ткани десны, фрагменты костей. В перспективе — новые проекты. Американские медики сообщают о пересадке «искусственных» уха и мочевого пузыря, шведы впервые в мире трансплантировали лабораторную вену. Французы испытали кровь из стволовых клеток.
Глаза, кишечник, легкие, предстательную железу, почки, сердце, печень и другие органы тоже выращивают. Но пока дальше экспериментов на животных не идут. Это технологии будущего, но, судя по всему, уже ближайшего.
МНЕНИЕ
Игорь ВОЛОТОВСКИЙ, директор Республиканского научно-медицинского центра «Клеточные технологии»:

Для выращивания органов нужны средства и кадры. Надо, чтобы наши увидели, как это делают в мире, освоили новые методики. Описывают, например, как можно вырастить сердце человека в организме свиньи. Это животное можно использовать в качестве биологического инкубатора, так как оно близко по иммунологическому статусу. Представим себе. Внутри оплодотворенной клетки свиньи образуется пул стволовых клеток. Потом из них получаются мезенхимальные стволовые. А они уже задают образование специализированных. В каждой эмбриональной клетке есть гены, отвечающие за формирование сердца как органа. Эти гены у свиньи уничтожают и в геном вставляют человеческие. В итоге сердце в организме свиньи развивается, но уже человеческое. Она вырастает до определенного возраста, после чего у нее забирают сердце и пересаживают. Реакция отторжения исключена, ведь больному пересаживают фактически его новое сердце. В Испании такие работы с недавних пор ведут. Если коллегам проект удастся, это будет переворот в трансплантологии. Думаю, по любым органам это можно делать, главное, хорошо знать геном.
Сергей РУБНИКОВИЧ, заведующий кафедрой ортопедической стоматологии и ортодонтии БелМАПО:

drug-olya@yandex.by
Фото Сергея ЛОЗЮКА, Виталия ПИВОВАРЧИКА